概述
在多種用於異源蛋白表達的系統和培養模式中,治療性抗體藥物的產業化製備始終以哺乳動物細胞大規模培養製程為主。其中中國倉鼠卵巢(CHO)細胞是用於治療性單克隆抗體生產的主要宿主,2016 年至今獲批上市的治療性抗體藥物全部為CHO細胞來源。但是在目前占主導地位的饋料批次培養製程中CHO細胞的新陳代謝遠未達到理想和最優狀態,其培養製程的建立需要大量的專業知識以及製程優化和過程監控。培養過程中具有毒性和抑制生長的代謝產物的產生和積累,是造成這種情況的主要原因之一。
在這些代謝產物中以乳酸和氨最具代表性,本文將就 CHO 細胞饋料批次培養中乳酸代謝的情況進行簡單整理,包括培養過程中乳酸的生成和消耗,乳酸代謝轉移發生的機制,影響和調控因素及其在製程開發中的應用。
(一)饋料批次培養中 CHO 細胞的生長及糖代謝特點
體外培養 CHO 細胞的代謝通常以效率低下和次優為特點,特徵是高效率吸收培養基中的葡萄糖和穀氨醯胺等底物作為碳源和氮源。
作為主要碳源的葡萄糖被細胞吸收並磷酸化為 6 磷酸葡萄糖(G6P),用於糖酵解生成三磷酸腺苷(ATP),還原型煙醯胺腺嘌呤二核苷酸(NADH)和丙酮酸。丙酮酸可以通過三羧酸迴圈徹底氧化為二氧化碳和水,釋放大量能量供細胞利用;也可以通過乳酸脫氫酶A(DHA)的作用與 NADH 的氧化一起轉化為乳酸。其中 35-70%的葡萄糖轉變為代謝廢物如乳酸,並對細胞培養性能發生不同程度的影響。
CHO 細胞饋料批次培養中的生長通常可以分為三個主要階段,即以細胞密度大幅度增加為主的對數生長期,細胞密度趨於穩定的穩定期,以及細胞密度和活率持續下降的凋亡期。
不同生長階段 CHO 細胞的代謝在很多方面會發生明顯變化,在這些代謝變化中乳酸從生成到消耗的轉移,是對饋料批次培養具有較大影響的是一個關鍵事件,與批次培養週期的延長、最終產物產量的提高等關係密切。
(二) CHO 細胞流饋料次培養中的乳酸代謝及其代謝轉移
乳酸是目前發現的 CHO 細胞培養中主要毒性代謝產物之一,可以引起培養環境的酸性變化,為了維持培養環境的酸堿恒定,需要通過補充鹼性物質對 pH 進行調節,而堿劑的補充則會引起滲透壓升高,抑制細胞生長,誘導細胞凋亡從而降低重組治療產品的生產率,某些情況下也會影響抗體產物的品質。
饋料批次培養中乳酸代謝通常會分為兩個不同階段:
對數期
在細胞快速生長的對數期,葡萄糖通過不完全氧化代謝滿足細胞快速增殖中對 ATP和脂肪酸的需求,葡萄糖的快速消耗伴隨著乳酸的大量產生。
穩定期
隨著細胞由快速生長進入穩定期,乳酸由生成轉變為消耗。乳酸從生成到消耗的代謝轉變,通常可以作為饋料批次培養製程中細胞代謝效率的標誌。
目標蛋白的高表達量與細胞培養中後期乳酸的代謝轉移呈強烈的正相關。缺乏有效的代謝轉移調控手段,是導致製程可變性增加的主要因素之一。加強對乳酸代謝的理解對於基於哺乳動物細胞培養的生物製程具有重要指導意義。當細胞快速增殖被突然打斷,糖酵解通量降低,及細胞外乳酸濃度升高等外部條件都可以觸發這種代謝轉移的發生。
(三) 乳酸代謝及其代謝轉移的影響及調節因素
饋料批次培養中細胞代謝的影響因素及調節策略很多,包括遺傳水準的影響及干預,細胞培養基組分的影響及調節,補料策略及培養環境的理化因素等。
01遺傳水準的干預
從遺傳水準對哺乳動物細胞培養中的乳酸代謝進行干預,是指基於細胞培養中的代謝通量研究和轉錄組學、代謝組學的結果,利用基因工程手段對代謝通路中的關鍵酶,進行基因水準的調整,製備出代謝特性改善的宿主細胞系。
通過轉錄組學及代謝通量研究發現,代謝轉移時細胞能量代謝相關的酶下調,但是還不足以由此引起代謝轉移。細胞外的高乳酸濃度,可以抑制糖酵解途徑的關鍵酶磷酸果糖激酶的活性,降低糖酵解代謝通量,促進乳酸向丙酮酸的轉化。在培養的後期,糖酵解活性調節的AKT1和P53信號通路的轉錄水準發生變化。
● 以往針對乳酸代謝調整的細胞工程化加工,重點集中在宿主細胞的固有基因的調節。
包括降低細胞乳酸脫氫酶的表達水準,促進丙酮酸進入線粒體;通過細胞轉運器調節細胞利用葡萄糖或葡萄糖替代物的能力;部分抑制乳酸脫氫酶A的基因,降低乳酸的產生以及葡萄糖的消耗,從而改善細胞生長;同時調節乳酸脫氫酶和3-磷酸甘油脫氫酶活性,改善細胞生長和表達;增加丙酮酸脫氫酶激酶活性減少乳酸積累並增加抗體產量等等。
● 近年來開始嘗試在細胞中引入外源基因,對乳酸代謝特性進行調節。
例如重組酵母丙酮酸羧化酶(Recombinant yeast pyruvate carboxylase PYC2)。
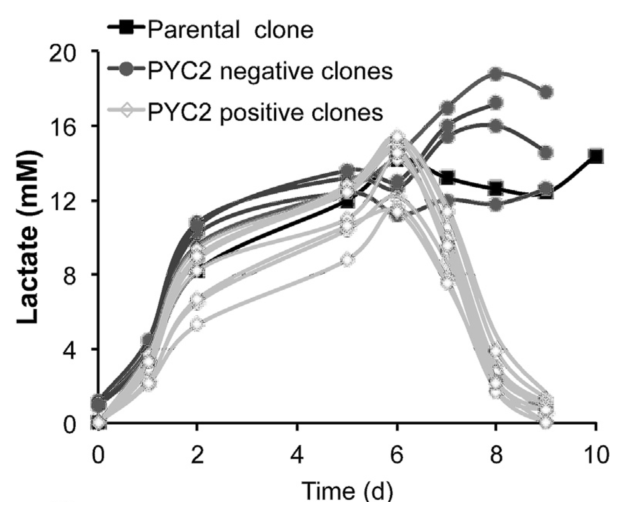
研究發現,穩定表達外源 PYC2 的 CHO 細胞來源的單抗表達克隆,在培養中傾向于向乳酸消耗的顯著和系統性代謝轉變,可有效延長細胞培養的對數生長期,提高細胞峰密度,進而增加抗體產物的表達量,見圖 1。
即使在高葡萄糖水平下,表達PYC2的CHO細胞克隆,在饋料批次培養中也能保持高效的代謝特性,從而降低了在細胞培養製程中為了避免乳酸堆積,而不得不將葡萄糖濃度控制在較低水準的必要,而因此減輕了培養中維持低水準葡萄糖對抗體產品糖基化的潛在負面影響。
在DG44細胞中引入丙酮酸羧化酶(hPC)基因,也可以導致乳酸生成的減少。此外,抗細胞凋亡基因可顯著改變CHO細胞的乳酸代謝,誘導向乳酸消耗的代謝轉變,並使最終抗體產量提高。
圖 1 外源酵母丙酮酸羧化酶2(PYC2)陽性克隆乳酸代謝改善明顯
02細胞培養基成分及補料策略
用於 CHO 細胞培養的無血清培養基通常富含葡萄糖和穀氨醯胺,是支援細胞快速生長所必需的,與永生化細胞中底物的部分氧化的代謝特性相關。即使有足夠的氧氣供應,葡萄糖依然通過部分氧化轉化為乳酸,而不是完全氧化為 CO2 和 H2O。
封面圖.png)